Introduction : Du laboratoire à la réalité clinique
La photobiomodulation transcrânienne (tPBM), issue de recherches prometteuses en laboratoire, trouve aujourd'hui des applications cliniques concrètes. Cette revue exhaustive examine les données probantes actuelles, en se concentrant sur les résultats quantifiables dans trois domaines essentiels : l’amélioration des fonctions cognitives chez les personnes en bonne santé, la prise en charge des maladies neurodégénératives et les effets bénéfiques sur le sommeil et la régulation de l’humeur.
La PBM agit principalement par l'activation de la cytochrome c oxydase, une enzyme mitochondriale essentielle. L'oxyde nitrique joue un rôle crucial dans la fonction mitochondriale en modulant l'activité de la cytochrome c oxydase, et la PBM peut amplifier la signalisation de l'oxyde nitrique, améliorant ainsi la respiration mitochondriale et la santé cellulaire.
Au niveau cellulaire, la photobiomodulation (PBM) influence divers processus, notamment la régulation des ions calcium, essentiels à la signalisation, à la prolifération et à la différenciation cellulaires. La PBM peut également activer des canaux ioniques photosensibles à des longueurs d'onde spécifiques, entraînant une augmentation de l'influx d'ions calcium et une modulation de l'activité neuronale.
Les modifications de l'expression génique et la différenciation des cellules souches sont en partie médiées par l'activation de facteurs de transcription via la PBM, ce qui induit une biogenèse mitochondriale accrue, une activité antioxydante renforcée et une réparation tissulaire. Plus précisément, il a été démontré que la PBM favorise la prolifération et la différenciation des cellules souches mésenchymateuses, contribuant ainsi à la régénération tissulaire.
Les mécanismes cellulaires sous-jacents à la PBM comprennent toute une série de mécanismes moléculaires, tels que la modulation de l'activité mitochondriale, la régulation de la production de cytokines et les modifications de l'expression génique.
Dans les maladies neurodégénératives, le dysfonctionnement mitochondrial est un facteur pathologique clé contribuant à la progression de la maladie. La photobiomodulation (PBM) cible ce dysfonctionnement en soutenant la fonction mitochondriale, en réduisant le stress oxydatif et en favorisant la survie neuronale.
L'inflammation est un autre domaine critique influencé par la PBM. Cette thérapie module la réponse inflammatoire en régulant les médiateurs de l'inflammation, tels que les cytokines et les chimiokines, qui jouent un rôle central dans la réparation tissulaire et la régulation immunitaire.
Les paramètres de la luminothérapie, notamment l'application d'un rayonnement lumineux à des longueurs d'onde spécifiques (telles que 810 nm et 905 nm), ont des effets significatifs sur les processus cellulaires comme la production de cytokines, l'activité des cellules immunitaires et la régénération des tissus.
Une dosimétrie appropriée est essentielle pour une PBM efficace, la densité d'énergie (mesurée en J/cm²) étant des facteurs clés qui déterminent les résultats biologiques et optimisent l'efficacité du traitement.
Les paramètres de l'appareil, tels que la puissance de sortie, sont essentiels pour garantir à la fois la sécurité et l'efficacité des appareils PBM, car ils influencent les effets thérapeutiques et minimisent les risques comme la surchauffe des tissus.
Les sources lumineuses utilisées en PBM comprennent la lumière rouge et la lumière proche infrarouge, chacune ayant des rôles distincts : la lumière rouge active principalement les voies mitochondriales à des profondeurs tissulaires plus superficielles, tandis que la lumière proche infrarouge pénètre plus profondément et est efficace pour activer la cytochrome c oxydase pour une production d’ATP accrue.
La LLLT peut également être administrée à l'aide de la technologie des diodes électroluminescentes (DEL), ce qui permet des applications multi-longueurs d'onde et un traitement ciblé des processus cellulaires, notamment la fonction mitochondriale et l'inflammation.
Cellules humaines et fonction cérébrale : les fondements biologiques
Les cellules humaines constituent l'élément fondamental de tous les tissus et organes, et leur santé est essentielle au fonctionnement optimal du cerveau. Dans le cerveau, des milliards de cellules spécialisées, appelées neurones, collaborent pour soutenir les processus cognitifs tels que la perception, la mémoire, l'attention et la prise de décision. La communication complexe entre ces cellules sous-tend tout, des informations sensorielles les plus élémentaires à la pensée et aux comportements les plus complexes.
Les progrès récents en matière de thérapie laser à faible intensité (LLLT) et de photobiomodulation (PBMT) ont révélé comment l'irradiation lumineuse ciblée peut influencer le comportement des cellules humaines, notamment dans le contexte des lésions cérébrales et des maladies neurodégénératives. La LLLT, qui utilise des lasers de faible intensité ou des diodes électroluminescentes, s'est avérée améliorer le métabolisme cellulaire, accélérer la cicatrisation et favoriser la réparation tissulaire. Par exemple, des recherches menées sur des fibroblastes embryonnaires de souris ont démontré que la thérapie laser peut augmenter la production d'ATP, réduire le stress oxydatif et stimuler le processus de cicatrisation au niveau cellulaire.
Un mécanisme moléculaire clé à l'origine de ces effets est l'activation de la cytochrome c oxydase, une enzyme essentielle de la chaîne respiratoire mitochondriale. Stimulée par l'irradiation laser, la cytochrome c oxydase augmente la production d'ATP, principale source d'énergie cellulaire. Cette augmentation d'énergie cellulaire soutient diverses fonctions vitales, de la prolifération cellulaire à la réparation des tissus endommagés. De plus, la thérapie par laser de faible intensité (LLLT) peut moduler la production d'espèces réactives de l'oxygène (ROS), qui agissent comme molécules de signalisation pour déclencher des processus cellulaires bénéfiques impliqués dans la régénération tissulaire et la réponse immunitaire.
Les cellules souches représentent un autre axe de recherche prometteur dans le domaine des fonctions cérébrales et de la réparation tissulaire. Ces cellules polyvalentes possèdent la capacité unique de se différencier en divers types cellulaires, notamment en neurones, ce qui les rend essentielles à la régénération tissulaire après un traumatisme crânien ou dans le contexte de maladies neurodégénératives. Des études ont montré que la thérapie par la lumière de faible intensité peut stimuler la prolifération et la différenciation des cellules souches, en partie en influençant leur mémoire épigénétique et l'expression de leurs gènes. Ainsi, le traitement laser pourrait aider à orienter les cellules souches vers les types cellulaires spécifiques nécessaires à la réparation et à la récupération cérébrales.
Les essais cliniques et les revues systématiques ont commencé à traduire ces découvertes cellulaires en bénéfices concrets. La thérapie par photobiomodulation a démontré des améliorations significatives des fonctions et des performances cognitives, notamment chez les personnes souffrant de troubles cognitifs ou de maladies comme la maladie d'Alzheimer. Ces thérapies ont également été associées à une réduction significative des cytokines inflammatoires, favorisant un environnement cérébral plus sain et pouvant potentiellement ralentir la progression des maladies neurodégénératives.
En résumé, l'interaction entre la luminothérapie et les cellules humaines constitue le fondement biologique de nombreux bénéfices cliniques observés avec la PBMT et la LLLT. En ciblant des mécanismes cellulaires tels que l'activation de la cytochrome c oxydase, la production d'ATP et la différenciation des cellules souches, ces thérapies offrent de nouvelles perspectives pour la réparation tissulaire, la cicatrisation et la restauration des fonctions cérébrales après un traumatisme ou en cas de maladie chronique. À mesure que la recherche progresse, une meilleure compréhension de ces processus cellulaires sera essentielle pour optimiser les protocoles de traitement et étendre le potentiel thérapeutique de la photobiomodulation en neurologie et au-delà.
Cliquez ici pour en savoir plus sur Fonction cérébrale optimale grâce à la tPBM
Amélioration cognitive chez les individus sains
Performances neuromusculaires et cognitives
Johnson et al. (2024) Une étude de validation de principe a été menée auprès de 43 participants (âgés de 18 à 69 ans) ayant des antécédents d'accélérations répétées de la tête. Après 8 semaines de traitement combiné par photobiomodulation (PBM) intranasale et transcrânienne à l'aide d'appareils Vielight, des améliorations significatives ont été observées
- Temps de réactionTaille de l'effet g = 0,75 (effet important). Amélioration substantielle de la vitesse de traitement sensorimoteur
- Contrôle de l'équilibre (MiniBEST)Taille de l'effet : g = 0,63 (effet moyen à important). Amélioration significative de la capacité à réagir aux troubles de l'équilibre
- Force de préhensiong = 0,22 (main dominante) et g = 0,34 (main non dominante). Amélioration de la force périphérique, suggérant des effets systémiques de la PBM cérébrale
Amélioration cognitive créative
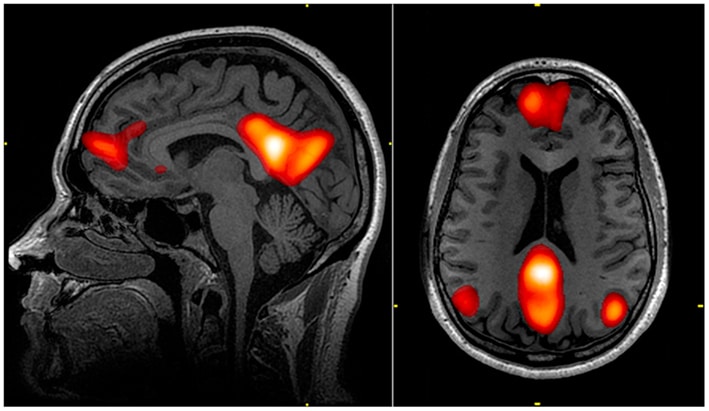
Peña et al. (2024) Cette étude a démontré que la photobiomodulation transcrânienne ciblant le réseau du mode par défaut améliorait la pensée créative divergente chez les adultes en bonne santé. Elle a mis en évidence des améliorations significatives concernant :
- Pensée divergente totale (DT): Rehaussement significatif (p = 0,004, η² = 0,24)
- Test d'utilisations inhabituellesAmélioration des scores de fluidité et d'originalité
- Test de complétion d'images: Indicateurs de performance améliorés
Cette recherche a utilisé une longueur d'onde de 810 nm avec une dosimétrie précise ciblant le cortex préfrontal, démontrant ainsi la capacité de la PBM à améliorer les fonctions cognitives au-delà des applications thérapeutiques.
Améliorations dans la prise en charge de la démence et des maladies neurodégénératives
Maladie d'Alzheimer et démence
Saltmarche et al. (2017) Ils ont publié la première série de cas complète documentant des améliorations cognitives significatives chez des patients atteints de démence légère à modérément sévère grâce aux dispositifs Vielight Neuro. Principaux résultats :
- Scores ADAS-cogAmélioration constante tout au long des 12 semaines de traitement, avec des bénéfices continus lors du suivi
- Inventaire neuropsychiatrique (NPI-FS)Améliorations comportementales significatives
- autonomie fonctionnelleAmélioration des activités de la vie quotidienne
- Profil de sécuritéAucun événement indésirable n'a été signalé chez tous les participants
Validation en neuroimagerie avancée
Chao (2019) ont mené un essai pilote randomisé démontrant des preuves cliniques et de neuroimagerie de l'efficacité de la PBM dans la démence :
Résultats cliniques :
- Amélioration des fonctions cognitives des systèmes ADASAmélioration cognitive statistiquement significative par rapport aux soins habituels
- Régulation comportementale: Mesuré par les améliorations de l'Inventaire Neuropsychiatrique
- Avantages durablesLes effets se sont maintenus pendant la période de suivi de 24 semaines
Preuves issues de la neuroimagerie :
- Augmentation de la perfusion cérébraleDémontré par IRM avec marquage de spin artériel
- Connectivité amélioréeAméliorations de la connectivité fonctionnelle dans le réseau en mode par défaut
- Préservation structurale: Progression de l'atrophie réduite par rapport aux témoins
Encéphalopathie traumatique chronique (ETC)
Naeser et al. Des améliorations remarquables ont été observées chez d'anciens joueurs de football présentant des symptômes probables d'encéphalopathie traumatique chronique après une thérapie par photobiomodulation transcrânienne :
Domaines cognitifs :
- Fonction exécutiveAméliorations significatives des performances au test de Stroop
- Amélioration de la mémoireAmélioration de l'apprentissage verbal et de la mémoire
- Régulation de l'attention: Augmentation de la capacité d'attention soutenue
Améliorations comportementales/de l'humeur :
- Symptômes du SSPTRéduction significative des scores PCL-C
- Gestion de la douleur: Diminution des scores de douleur SF-MPQ
- qualité du sommeilAmélioration des scores PSQI
Preuves issues d'une revue systématique
UN revue systématique exhaustive (Lim, 2024) Sept études cliniques sur la maladie d'Alzheimer présentant des résultats cohérents ont été identifiées :
- Profil de sécurité universelAucun événement indésirable n'a été rapporté dans les études
- Améliorations cognitivesAméliorations constantes dans les domaines de la mémoire et de la cognition
- Paramètres hétérogènesLes études variaient en longueur d'onde (660-1070 nm), en densité de puissance et en durée de traitement
- Signification clinique: Tailles d'effet allant de faibles à importantes selon les mesures cognitives
Bienfaits pour la qualité du sommeil et la régulation de l'humeur
Améliorations de l'architecture du sommeil
Zhao et al. (2022) ont mené une étude randomisée contrôlée par placebo démontrant des améliorations significatives de la qualité du sommeil dans le déclin cognitif subjectif :
- Indice de qualité du sommeil de Pittsburgh (PSQI)Améliorations significatives par rapport au groupe témoin
- efficacité du sommeilParamètres d'architecture du sommeil améliorés
- Qualité subjective du sommeilAméliorations de la satisfaction du sommeil rapportées par les patients
Mécanismes neurochimiques
La recherche démontre l'influence de la PBM sur les voies neurochimiques liées au sommeil :
Régulation circadienne :
- Régulation améliorée de la production de mélatonine
- Amélioration de la synchronisation du rythme circadien
- Stabilité optimisée du cycle veille-sommeil
Modulation des neurotransmetteurs :
- Augmentation de la disponibilité de la sérotonine et de la dopamine
- Fonctionnement amélioré du système GABA
- Réduction des taux de cortisol et d'hormones de stress
Régulation de l'humeur et du stress
De nombreuses études documentent les effets d'amélioration de l'humeur :
Dépression et anxiété :
- Améliorations significatives des scores à l'inventaire de dépression de Beck
- Diminution de l'anxiété mesurée sur plusieurs échelles d'évaluation
- Capacité accrue de régulation émotionnelle
Réponse au stress :
- Amélioration de la variabilité de la fréquence cardiaque
- Réduction des marqueurs inflammatoires (IL-6, TNF-α)
- Mesures renforcées de résilience au stress
Paramètres techniques pour des résultats optimaux
Spécifications du dispositif Vielight Neuro
Paramètres d'éclairage :
- Longueur d'onde: 810 nm (proche infrarouge)
- Densité de puissance: 100-300 mW/cm²
- Fréquence d'impulsionModes 10 Hz (Alpha) et 40 Hz (Gamma)
- Durée du traitement: 20 minutes par séance
- Dosimétrie: dose de 60 J/cm² au niveau du cuir chevelu permettant d'atteindre une dose neuronale de 5 à 10 J/cm²
Optimisation des protocoles fondée sur des données probantes
Les recherches suggèrent que les paramètres optimaux incluent :
- FréquenceAu moins 3 fois par semaine pour des effets durables
- Durée: Protocoles de traitement initiaux de 8 à 12 semaines
- EntretienDes séances régulières sont nécessaires pour obtenir des bénéfices durables dans les maladies neurodégénératives
- IndividualisationAjustement des paramètres en fonction du retour d'information de l'EEG et de la réponse clinique
Orientations futures de la recherche et implications cliniques
Limites actuelles de la recherche
- Tailles des échantillonsLa plupart des études portent sur de petites cohortes (4 à 57 participants)
- hétérogénéité des paramètresVariabilité de la longueur d'onde, du dosage et des protocoles
- Besoins de normalisation: Exigence de mesures d'évaluation unifiées
- Études à long termeNécessité de périodes de suivi prolongées
Applications émergentes
Protocoles guidés par EEG :
- Surveillance en temps réel de l'état cérébral pour l'optimisation des paramètres
- Sélection personnalisée des fréquences en fonction des rythmes cérébraux individuels
- Personnalisation des traitements par l'IA
Thérapies combinées :
- Effets synergiques avec l'entraînement par neurofeedback
- Intégration aux interventions cognitivo-comportementales
- Approches de neuromodulation multimodales
Considérations relatives à la mise en œuvre clinique
Sécurité et contre-indications
Profil de sécurité établi :
- Aucun événement indésirable grave n'a été rapporté dans la littérature publiée
- Effets secondaires légers et temporaires : fatigue, maux de tête, gorge sèche (disparaissent généralement en 1 à 2 séances)
- Contre-indications : Hémorragie cérébrale active, antécédents de convulsions, grossesse
Statut réglementaire
Classification actuelle :
- La FDA les a classés comme « dispositifs de bien-être général à faible risque »
- Certification de sécurité TÜV pour l'usage des consommateurs
- Non approuvé pour les demandes de remboursement de traitements médicaux spécifiques
- L'application clinique requiert un consentement éclairé approprié et une supervision professionnelle
En résumé : Mise en œuvre fondée sur des données probantes
Les données cliniques relatives à la photobiomodulation transcrânienne démontrent des bénéfices constants et mesurables dans les domaines cognitif, comportemental et neurophysiologique. Principaux enseignements pour la pratique clinique :
- Profil de sécurité robusteDes recherches approfondies confirment un risque minimal avec des protocoles appropriés
- Efficacité mesurable: Tailles d'effet allant de faibles à importantes pour de multiples mesures de résultats
- Applications généralesDes bénéfices ont été démontrés dans le cadre de l'amélioration de la santé et dans un contexte thérapeutique
- Précision techniqueDes résultats optimaux nécessitent une sélection des paramètres et une dosimétrie fondées sur des données probantes
- Intégration professionnelleLes meilleurs bénéfices sont obtenus dans le cadre de protocoles de neurothérapie complets
Pour les clients de Neurofeedback Luxembourg, la tPBM représente un ajout scientifiquement validé à notre gamme de neurothérapies, offrant des avantages uniques en matière d'optimisation cérébrale et de protocoles d'intervention thérapeutique.
Cette revue synthétise les recherches publiées dans des revues à comité de lecture jusqu'en janvier 2025. Les résultats individuels peuvent varier. Une consultation professionnelle est recommandée pour les applications thérapeutiques.
Découvrez dès aujourd'hui le potentiel d'optimisation de votre cerveau. Visitez notre site web pour en savoir plus photobiomodulation et notre approche intégrée, et planifiez votre téléconsultation préliminaireEnsemble, explorons comment la photobiomodulation transcrânienne peut transformer votre santé cérébrale.
Références
Chao, LL (2019). Effets des traitements de photobiomodulation à domicile sur la fonction cognitive et comportementale, la perfusion cérébrale et la connectivité fonctionnelle au repos chez les patients atteints de démence : un essai pilote. Photobiomodulation, photomédecine et chirurgie laser, 37(3), 133‑141. https://doi.org/10.1089/photob.2018.4555
Graner, J., Oakes, TR, French, LM et Riedy, G. (2013). L'IRM fonctionnelle dans l'étude des traumatismes crâniens liés aux explosions. Frontières en neurologie, 4, 16. https://doi.org/10.3389/fneur.2013.00016
Johnson, PK, Fino, PC, Wilde, EA, Hovenden, ES, Russell, HA, Velez, C., Pelo, R., Morris, AJ, Kreter, N., Read, EN, Keleher, F., Esopenko, C., Lindsey, HM, Newsome, MR, Thayn, D., McCabe, C., Mullen, CM, Davidson, LE, Liebel, SW, … Tate, DF (2024). L'effet de la photobiomodulation intranasale et transcrânienne sur le contrôle neuromusculaire chez les individus présentant des événements d'accélération de la tête répétitifs. Photobiomodulation, photomédecine et chirurgie laser, 42(6), 404‑413. https://doi.org/10.1089/pho.2023.0178
Lim, L. (2024). Modification de la physiopathologie de la maladie d'Alzheimer par photobiomodulation : Modèle, preuves et avenir avec une intervention guidée par EEG. Frontières en neurologie, 15. https://doi.org/10.3389/fneur.2024.1407785
Naeser, MA, Martin, PI, Ho, MD, Krengel, MH, Bogdanova, Y., Knight, JA, Hamblin, MR, Fedoruk, AE, Poole, LG, Cheng, C., & Koo, B. (sd). Traitement par photobiomodulation transcrânienne : Améliorations significatives chez quatre anciens joueurs de football atteints d'encéphalopathie traumatique chronique possible. Journal des rapports sur la maladie d'Alzheimer, 7(1), 77‑105. https://doi.org/10.3233/ADR-220022
Peña, J., Muthalib, M., Beaty, RE, Sampedro, A., Ibarretxe-Bilbao, N., Zubiaurre-Elorza, L., García-Guerrero, MA, Cortazar, I., Niso, M. et Ojeda, N. (2024). Amélioration de la pensée créative divergente après la photobiomodulation transcrânienne dans le proche infrarouge sur le réseau en mode par défaut. Journal de recherche sur la créativité, 36(1), 1‑14. https://doi.org/10.1080/10400419.2023.2219953
Saltmarche, AE, Naeser, MA, Ho, KF, Hamblin, MR et Lim, L. (2017). Amélioration significative de la cognition dans les cas de démence légère à modérément sévère traités par photobiomodulation transcrânienne et intranasale : rapport de série de cas. Photomédecine et chirurgie laser, 35(8), 432‑441. https://doi.org/10.1089/pho.2016.4227
Zhao, C., Li, D., Kong, Y., Liu, H., Hu, Y., Niu, H., Jensen, O., Li, X., Liu, H., & Song, Y. (sd). La photobiomodulation transcrânienne améliore la capacité de la mémoire de travail visuelle chez l'homme. Progrès scientifiques, 8(48), eabq3211. https://doi.org/10.1126/sciadv.abq3211

