Einleitung: Vom Labor zur klinischen Realität
Die transkranielle Photobiomodulation (tPBM) hat sich aus vielversprechender Laborforschung zu nachweisbaren klinischen Anwendungen entwickelt. Diese umfassende Übersicht untersucht die aktuelle Evidenzbasis und konzentriert sich auf quantifizierbare Ergebnisse in drei kritischen Bereichen: kognitive Verbesserung bei gesunden Menschen, Behandlung neurodegenerativer Erkrankungen und Vorteile bei der Regulierung von Schlaf und Stimmung.
PBM wirkt hauptsächlich durch die Aktivierung der Cytochrom-c-Oxidase, einem wichtigen mitochondrialen Enzym. Stickstoffmonoxid spielt eine entscheidende Rolle für die mitochondriale Funktion, indem es die Cytochrom-c-Oxidase-Aktivität moduliert. PBM kann die Stickoxid-Signalgebung verstärken und so die mitochondriale Atmung und die Zellgesundheit verbessern.
Auf zellulärer Ebene beeinflusst PBM eine Vielzahl von Prozessen, darunter die Regulierung von Calciumionen, die für die Zellsignalisierung, Proliferation und Differenzierung essentiell sind. PBM kann auch lichtempfindliche Ionenkanäle bei bestimmten Wellenlängen aktivieren, was zu einem erhöhten Calciumioneneinstrom und einer Modulation der neuronalen Aktivität führt.
Veränderungen der Genexpression und die Differenzierung von Stammzellen werden teilweise durch die Aktivierung von Transkriptionsfaktoren durch PBM vermittelt, was zu einer verbesserten mitochondrialen Biogenese, antioxidativer Aktivität und Gewebereparatur führt. Insbesondere fördert PBM nachweislich die Proliferation und Differenzierung mesenchymaler Stammzellen und unterstützt so die Geweberegeneration.
Zu den zellulären Mechanismen, die PBM zugrunde liegen, gehören eine Reihe molekularer Mechanismen, wie etwa die Modulation der mitochondrialen Aktivität, die Regulierung der Zytokinproduktion und Veränderungen der Genexpression.
Bei neurodegenerativen Erkrankungen ist die mitochondriale Dysfunktion ein wichtiger pathologischer Faktor, der zum Fortschreiten der Krankheit beiträgt. PBM zielt auf diese Dysfunktion ab, indem es die mitochondriale Funktion unterstützt, oxidativen Stress reduziert und das neuronale Überleben fördert.
Entzündungen sind ein weiterer kritischer Bereich, der von PBM beeinflusst wird. Die Therapie moduliert die Entzündungsreaktion durch die Regulierung von Entzündungsmediatoren wie Zytokinen und Chemokinen, die eine zentrale Rolle bei der Gewebereparatur und Immunregulation spielen.
Die Parameter der Lichttherapie, einschließlich der Anwendung von Lichtstrahlung bei bestimmten Wellenlängen (wie 810 nm und 905 nm), haben erhebliche Auswirkungen auf zelluläre Prozesse wie die Zytokinproduktion, die Aktivität von Immunzellen und die Geweberegeneration.
Eine ordnungsgemäße Dosimetrie ist für eine wirksame PBM von entscheidender Bedeutung, wobei die Energiedichte und die Energiedichten (gemessen in J/cm²) Schlüsselfaktoren sind, die die biologischen Ergebnisse bestimmen und die Wirksamkeit der Behandlung optimieren.
Geräteparameter wie die Leistungsabgabe sind für die Gewährleistung der Sicherheit und Wirksamkeit von PBM-Geräten von entscheidender Bedeutung, da sie die therapeutische Wirkung beeinflussen und Risiken wie eine Überhitzung des Gewebes minimieren.
Zu den bei PBM verwendeten Lichtquellen zählen Rotlicht und Nahinfrarotlicht, die jeweils unterschiedliche Aufgaben erfüllen: Rotlicht aktiviert vor allem mitochondriale Bahnen in geringerer Gewebetiefe, während Nahinfrarotlicht tiefer eindringt und die Cytochrom-c-Oxidase zur Steigerung der ATP-Produktion wirksam aktiviert.
LLLT kann auch mithilfe der Leuchtdiodentechnologie (LED) durchgeführt werden, die Anwendungen mit mehreren Wellenlängen und eine gezielte Behandlung zellulärer Prozesse, einschließlich der mitochondrialen Funktion und Entzündungen, ermöglicht.
Menschliche Zellen und Gehirnfunktion: Die biologische Grundlage
Menschliche Zellen sind die Bausteine aller Gewebe und Organe, und ihre Gesundheit ist grundlegend für eine optimale Gehirnfunktion. Im Gehirn arbeiten Milliarden spezialisierter Zellen, sogenannte Neuronen, zusammen, um kognitive Prozesse wie Wahrnehmung, Gedächtnis, Aufmerksamkeit und Entscheidungsfindung zu unterstützen. Die komplexe Kommunikation zwischen diesen Zellen bildet die Grundlage für alles, von einfachen Sinneseindrücken bis hin zu komplexen Gedanken und Verhaltensweisen.
Jüngste Fortschritte in der Low-Level-Lasertherapie (LLLT) und der Photobiomodulationstherapie (PBMT) haben gezeigt, wie gezielte Lichtbestrahlung das Verhalten menschlicher Zellen beeinflussen kann, insbesondere im Zusammenhang mit Hirnverletzungen und neurodegenerativen Erkrankungen. LLLT, bei der Laser mit geringer Intensität oder Leuchtdioden zum Einsatz kommen, verbessert nachweislich den Zellstoffwechsel, beschleunigt die Wundheilung und fördert die Gewebereparatur. Beispielsweise hat die Forschung an embryonalen Fibroblasten von Mäusen gezeigt, dass Lasertherapie die ATP-Produktion steigern, oxidativen Stress reduzieren und den Heilungsprozess auf zellulärer Ebene stimulieren kann.
Ein wichtiger molekularer Mechanismus hinter diesen Effekten ist die Aktivierung der Cytochrom-c-Oxidase, einem wichtigen Enzym in der mitochondrialen Atmungskette. Durch Laserbestrahlung stimuliert, steigert die Cytochrom-c-Oxidase die Produktion von ATP, dem primären Energieträger der Zelle. Dieser Anstieg der Zellenergie unterstützt eine Reihe lebenswichtiger Funktionen, von der Zellproliferation bis zur Reparatur geschädigten Gewebes. Darüber hinaus kann LLLT die Produktion reaktiver Sauerstoffspezies (ROS) modulieren, die als Signalmoleküle nützliche zelluläre Prozesse auslösen, die an der Geweberegeneration und Immunantwort beteiligt sind.
Stammzellen sind ein weiteres vielversprechendes Forschungsgebiet im Bereich der Gehirnfunktion und Gewebereparatur. Diese vielseitigen Zellen besitzen die einzigartige Fähigkeit, sich in verschiedene Zelltypen, einschließlich Neuronen, zu differenzieren. Dadurch sind sie für die Geweberegeneration nach traumatischen Hirnverletzungen oder im Zusammenhang mit neurodegenerativen Erkrankungen unverzichtbar. Studien haben gezeigt, dass Low-Level-Lichttherapie die Proliferation und Differenzierung von Stammzellen fördern kann, unter anderem durch Beeinflussung des epigenetischen Gedächtnisses und der Genexpression von Stammzellen. Dies bedeutet, dass eine Laserbehandlung dazu beitragen kann, Stammzellen zu den spezifischen Zelltypen zu entwickeln, die für die Reparatur und Genesung des Gehirns benötigt werden.
Klinische Studien und systematische Übersichtsarbeiten haben begonnen, diese zellulären Erkenntnisse in praktische Vorteile umzusetzen. Die Photobiomodulationstherapie hat signifikante Verbesserungen der kognitiven Funktion und Leistungsfähigkeit gezeigt, insbesondere bei Personen mit kognitiven Beeinträchtigungen oder Erkrankungen wie Alzheimer. Diese Therapien werden auch mit einer signifikanten Reduktion entzündlicher Zytokine in Verbindung gebracht, was zu einer gesünderen Gehirnumgebung beiträgt und möglicherweise das Fortschreiten neurodegenerativer Erkrankungen verlangsamt.
Zusammenfassend lässt sich sagen, dass die Interaktion zwischen Lichttherapie und menschlichen Zellen die biologische Grundlage für viele der klinischen Vorteile von PBMT und LLLT bildet. Durch die gezielte Aktivierung zellulärer Mechanismen wie der Aktivierung der Cytochrom-c-Oxidase, der ATP-Produktion und der Stammzelldifferenzierung bieten diese Therapien neue Hoffnung für Gewebereparatur, Wundheilung und die Wiederherstellung der Gehirnfunktion nach Verletzungen oder bei chronischen Erkrankungen. Im weiteren Verlauf der Forschung wird ein tieferes Verständnis dieser zellulären Prozesse für die Optimierung von Behandlungsprotokollen und die Erweiterung des therapeutischen Potenzials der Photobiomodulation in der Neurologie und darüber hinaus von entscheidender Bedeutung sein.
Klicken Sie hier, um mehr zu erfahren über Optimale Gehirnfunktion mit tPBM
Kognitive Verbesserung bei gesunden Personen
Neuromuskuläre und kognitive Leistung
Johnson et al. (2024) führte eine Proof-of-Concept-Studie mit 43 Teilnehmern (im Alter von 18 bis 69 Jahren) durch, die in der Vergangenheit wiederholt Kopfbeschleunigungsereignisse aufwiesen. Nach 8 Wochen kombinierter intranasaler und transkranieller PBM-Therapie mit Vielight-Geräten wurden signifikante Verbesserungen dokumentiert:
- Reaktionszeit: Effektstärke g = 0,75 (großer Effekt). Deutliche Verbesserung der sensorisch-motorischen Verarbeitungsgeschwindigkeit
- Gleichgewichtskontrolle (MiniBEST): Effektstärke g = 0,63 (mittelgroßer Effekt). Signifikante Verbesserung der Reaktionsfähigkeit auf Gleichgewichtsstörungen
- Griffstärke: g = 0,22 (dominante) und g = 0,34 (nicht-dominante Hand). Verbesserung der peripheren Kraft, was auf systemische Effekte der zerebralen PBM hindeutet
Kreative kognitive Verbesserung
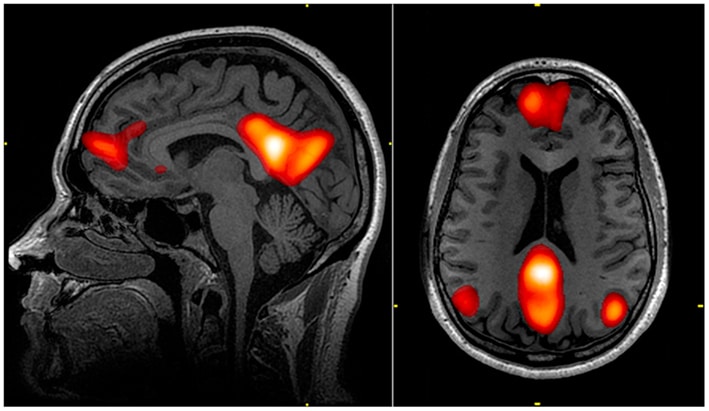
Peña et al. (2024) zeigte, dass die transkranielle Photobiomodulation über das Ruhezustandsnetzwerk das divergentes kreative Denken bei gesunden Erwachsenen förderte. Die Studie zeigte signifikante Verbesserungen in:
- Total divergentes Denken (DT): Signifikante Verbesserung (p = 0,004, η² = 0,24)
- Test für ungewöhnliche Verwendungen: Verbesserte Ergebnisse bei Flüssigkeit und Originalität
- Bildvervollständigungstest: Verbesserte Leistungsmetriken
Bei der Forschung wurde eine Wellenlänge von 810 nm mit präziser Dosimetrie verwendet, die auf den präfrontalen Kortex abzielte. Dies demonstrierte das Potenzial von PBM zur kognitiven Verbesserung über therapeutische Anwendungen hinaus.
Verbesserungen bei Demenz und neurodegenerativen Erkrankungen
Alzheimer-Krankheit und Demenz
Saltmarche et al. (2017) veröffentlichte die erste abgeschlossene Fallserie, die signifikante kognitive Verbesserungen bei leichter bis mittelschwerer Demenz durch den Einsatz von Vielight Neuro-Geräten dokumentiert. Zu den wichtigsten Ergebnissen gehörten:
- ADAS-cog-Ergebnisse: Anhaltende Verbesserung während der 12-wöchigen Behandlungsdauer, mit anhaltenden Vorteilen während der Nachuntersuchung
- Neuropsychiatrisches Inventar (NPI-FS): Deutliche Verhaltensverbesserungen
- Funktionale Unabhängigkeit: Verbesserte Aktivitäten des täglichen Lebens
- Sicherheitsprofil: Keine unerwünschten Ereignisse bei allen Teilnehmern gemeldet
Erweiterte Validierung der Neurobildgebung
Chao (2019) führte eine randomisierte Pilotstudie durch, die sowohl klinische als auch bildgebende Beweise für die Wirksamkeit von PBM bei Demenz lieferte:
Klinische Ergebnisse:
- ADAS-Zahnradverbesserung: Statistisch signifikante kognitive Verbesserung im Vergleich zur üblichen Behandlung
- Verhaltensregulierung: Gemessen über Verbesserungen des Neuropsychiatrischen Inventars
- Nachhaltige Vorteile: Effekte blieben während der 24-wöchigen Nachbeobachtungszeit erhalten
Nachweise durch Neuroimaging:
- Erhöhte zerebrale Durchblutung: Nachgewiesen durch arterielle Spinmarkierung MRI
- Verbesserte Konnektivität: Funktionale Konnektivitätsverbesserungen im Standardmodusnetzwerk
- Bauliche Erhaltung: Reduzierte Atrophieprogression im Vergleich zu Kontrollen
Chronische traumatische Enzephalopathie (CTE)
Naeser et al. berichteten über bemerkenswerte Verbesserungen bei ehemaligen Footballspielern mit wahrscheinlichen CTE-Symptomen nach transkranieller PBM-Therapie:
Kognitive Domänen:
- Exekutive Funktion: Signifikante Verbesserungen bei der Leistung des Stroop-Tests
- Gedächtnisverbesserung: Verbesserungen beim verbalen Lernen und Gedächtnis
- Aufmerksamkeitsregulierung: Die anhaltende Aufmerksamkeitskapazität steigt
Verhaltens-/Stimmungsverbesserungen:
- PTBS-Symptome: Signifikante Reduzierung der PCL-C-Werte
- Schmerzbehandlung: Verringerte SF-MPQ-Schmerzwerte
- Schlafqualität: Verbesserte PSQI-Ergebnisse
Systematische Überprüfung der Evidenz
A umfassende systematische Überprüfung (Lim, 2024) identifizierte sieben klinische Studien zur Alzheimer-Krankheit mit übereinstimmenden Ergebnissen:
- Universelles Sicherheitsprofil: In allen Studien wurden keine unerwünschten Ereignisse berichtet
- Kognitive Verbesserungen: Kontinuierliche Verbesserungen in den Bereichen Gedächtnis und Kognition
- Heterogene Parameter: Die Studien variierten hinsichtlich Wellenlänge (660–1070 nm), Leistungsdichte und Behandlungsdauer
- Klinische Bedeutung: Effektstärken von klein bis groß über kognitive Messungen hinweg
Vorteile für die Schlafqualität und Stimmungsregulierung
Verbesserungen der Schlafarchitektur
Zhao et al. (2022) führte eine randomisierte, Schein-kontrollierte Studie durch, die signifikante Verbesserungen der Schlafqualität bei subjektivem kognitivem Abbau zeigte:
- Pittsburgh Schlafqualitätsindex (PSQI): Signifikante Verbesserungen im Vergleich zur Scheinkontrolle
- Schlafeffizienz: Verbesserte Schlafarchitekturparameter
- Subjektive Schlafqualität: Von Patienten berichtete Verbesserungen der Schlafzufriedenheit
Neurochemische Mechanismen
Untersuchungen belegen den Einfluss von PBM auf schlafbezogene neurochemische Bahnen:
Zirkadiane Regulierung:
- Verbesserte Regulierung der Melatoninproduktion
- Verbesserte Synchronisierung des zirkadianen Rhythmus
- Optimierte Schlaf-Wach-Rhythmus-Stabilität
Neurotransmittermodulation:
- Erhöhte Verfügbarkeit von Serotonin und Dopamin
- Verbesserte Funktion des GABA-Systems
- Reduzierter Cortisol- und Stresshormonspiegel
Stimmungs- und Stressregulierung
Mehrere Studien belegen stimmungsaufhellende Effekte:
Depression und Angst:
- Signifikante Verbesserungen bei den Werten des Beck-Depressions-Inventars
- Reduzierte Angstwerte über mehrere Bewertungsskalen hinweg
- Verbesserte Fähigkeit zur emotionalen Regulierung
Stressreaktion:
- Verbesserte Herzfrequenzvariabilität
- Reduzierte Entzündungsmarker (IL-6, TNF-α)
- Verbesserte Maßnahmen zur Stressresistenz
Technische Parameter für optimale Ergebnisse
Spezifikationen des Vielight Neuro-Geräts
Lichtparameter:
- Wellenlänge: 810 nm (Nahinfrarot)
- Leistungsdichte: 100-300 mW/cm²
- Pulsfrequenz: 10 Hz (Alpha) und 40 Hz (Gamma) Modi
- Behandlungsdauer: 20 Minuten pro Sitzung
- Dosimetrie: 60 J/cm² Kopfhautdosis, die eine neuronale Dosis von 5-10 J/cm² erreicht
Evidenzbasierte Protokolloptimierung
Untersuchungen legen nahe, dass zu den optimalen Parametern gehören:
- Frequenz: Mindestens 3 Mal pro Woche für anhaltende Wirkung
- Dauer: 8-12 Wochen Erstbehandlungsprotokolle
- Wartung: Für anhaltende Vorteile bei neurodegenerativen Erkrankungen sind fortlaufende Sitzungen erforderlich
- Individualisierung: Parameteranpassung basierend auf EEG-Feedback und klinischer Reaktion
Zukünftige Forschungsrichtungen und klinische Implikationen
Aktuelle Forschungsbeschränkungen
- Stichprobengrößen: Die meisten Studien umfassen kleine Kohorten (4-57 Teilnehmer)
- Parameterheterogenität: Variabilität in Wellenlänge, Dosierung und Protokollen
- Standardisierungsbedarf: Forderung nach einheitlichen Bewertungsmaßstäben
- Langzeitstudien: Notwendigkeit längerer Nachbeobachtungszeiträume
Neue Anwendungen
EEG-gesteuerte Protokolle:
- Echtzeitüberwachung des Gehirnzustands zur Parameteroptimierung
- Personalisierte Frequenzauswahl basierend auf individuellen Gehirnrhythmen
- KI-gesteuerte Behandlungsanpassung
Kombinationstherapien:
- Synergieeffekte mit Neurofeedback-Training
- Integration mit kognitiven Verhaltensinterventionen
- Multimodale Neuromodulationsansätze
Überlegungen zur klinischen Implementierung
Sicherheit und Kontraindikationen
Festgelegtes Sicherheitsprofil:
- Keine schwerwiegenden unerwünschten Ereignisse in der veröffentlichten Literatur
- Leichte vorübergehende Nebenwirkungen: Müdigkeit, Kopfschmerzen, trockener Hals (klingen normalerweise innerhalb von 1–2 Sitzungen ab)
- Kontraindikationen: Aktive Hirnblutungen, Krampfanfälle in der Anamnese, Schwangerschaft
Regulatorischer Status
Aktuelle Klassifizierung:
- Von der FDA als „allgemeine Wellnessgeräte mit geringem Risiko“ eingestuft
- TÜV-Sicherheitszertifizierung für den Privatgebrauch
- Nicht für spezifische medizinische Behandlungsansprüche zugelassen
- Klinische Anwendung erfordert entsprechende Einverständniserklärung und professionelle Aufsicht
Fazit: Evidenzbasierte Umsetzung
Die klinische Evidenz für die transkranielle Photobiomodulation zeigt konsistente, messbare Vorteile in kognitiven, verhaltensbezogenen und neurophysiologischen Bereichen. Wichtige Erkenntnisse für die klinische Praxis:
- Robustes Sicherheitsprofil: Umfangreiche Forschung bestätigt minimales Risiko bei ordnungsgemäßen Protokollen
- Messbare Wirksamkeit: Effektstärken von klein bis groß über mehrere Ergebnismaße hinweg
- Breite Anwendungsmöglichkeiten: Vorteile sowohl im gesundheitsfördernden als auch im therapeutischen Kontext nachgewiesen
- Technische Präzision: Optimale Ergebnisse erfordern eine evidenzbasierte Parameterauswahl und Dosimetrie
- Berufliche Integration: Größter Nutzen im Rahmen umfassender Neurotherapie
Für Kunden von Neurofeedback Luxembourg stellt tPBM eine wissenschaftlich validierte Ergänzung unseres Neurotherapie-Angebots dar und bietet einzigartige Vorteile bei der Gehirnoptimierung und bei therapeutischen Interventionsprotokollen.
Dieser Bericht fasst aktuelle, von Experten begutachtete Forschungsergebnisse bis Januar 2025 zusammen. Individuelle Ergebnisse können abweichen. Für therapeutische Anwendungen wird eine professionelle Beratung empfohlen.
Entdecken Sie noch heute Ihr Gehirnoptimierungspotenzial. Besuchen Sie unsere Website, um mehr zu erfahren über Photobiomodulation und unser integrierter Ansatz und planen Sie Ihre Vorläufige Teleconsultation. Lassen Sie uns zusammen untersuchen, wie die transkranielle Photobiomodulation Ihre Gesundheit des Gehirns verändern kann.
Referenzen
Chao, LL (2019). Auswirkungen von Photobiomodulationsbehandlungen häuslicher Behandlungen auf die kognitive und verhaltensbezogene Funktion, die zerebrale Perfusion und die funktionelle Konnektivität von Ruhezustand bei Patienten mit Demenz: eine Pilotstudie. Photobiomodulation, Photomedizin und Laserchirurgie, 37(3), 133‑141. https://doi.org/10.1089/photob.2018.4555
Graner, J., Oakes, TR, French, LM, & Riedy, G. (2013). Funktionelle MRT bei der Untersuchung von explosionsbedingten traumatischen Hirnverletzungen. Grenzen der Neurologie, 4, 16. https://doi.org/10.3389/fneur.2013.00016
Johnson, PK, Fino, PC, Wilde, EA, Hovenden, ES, Russell, HA, Velez, C., Pelo, R., Morris, AJ, Kreter, N., Read, EN, Keleher, F., Esopenko, C., Lindsey, HM, Newsome, MR, Thayn, D., McCabe, C., Mullen, CM, Davidson, LE, Liebel, SW, … Tate, DF (2024). Die Wirkung der intranasalen und transkraniellen Photobiomodulation auf die neuromuskuläre Kontrolle bei Personen mit wiederholten Kopfbeschleunigungsereignissen. Photobiomodulation, Photomedizin und Laserchirurgie, 42(6), 404‑413. https://doi.org/10.1089/pho.2023.0178
Lim, L. (2024). Modifizierung der Pathophysiologie der Alzheimer-Krankheit durch Photobiomodulation: Modell, Beweise und Zukunft mit EEG-gesteuerter Intervention. Grenzen der Neurologie, 15. https://doi.org/10.3389/fneur.2024.1407785
Naeser, MA, Martin, PI, Ho, MD, Krengel, MH, Bogdanova, Y., Knight, JA, Hamblin, MR, Fedoruk, AE, Poole, LG, Cheng, C., & Koo, B. (sd). Transkranielle Photobiomodulationsbehandlung: Signifikante Verbesserungen bei vier ehemaligen Footballspielern mit möglicher chronischer traumatischer Enzephalopathie. Journal of Alzheimer's Disease Reports, 7(1), 77‑105. https://doi.org/10.3233/ADR-220022
Peña, J., Muthalib, M., Beaty, RE, Sampedro, A., Ibarretxe-Bilbao, N., Zubiaurre-Elorza, L., García-Guerrero, MA, Cortazar, I., Niso, M. & Ojeda, N. (2024). Verbesserung des divergenten kreativen Denkens nach transkranieller Nahinfrarot-Photobiomodulation über das Standardmodus-Netzwerk. Kreativitätsforschungsjournal, 36(1), 1‑14. https://doi.org/10.1080/10400419.2023.2219953
Saltmarchche, AE, Naeser, MA, Ho, KF, Hamblin, MR, Lim, L. (2017). Eine signifikante Verbesserung der Kognition in mild bis mäßig schweren Demenzfällen, die mit transkranieller und intranasaler Photobiomodulation behandelt wurden: Fallreihenbericht. Photomedizin und Laserchirurgie, 35(8), 432‑441. https://doi.org/10.1089/pho.2016.4227
Zhao, C., Li, D., Kong, Y., Liu, H., Hu, Y., Niu, H., Jensen, O., Li, X., Liu, H., & Song, Y. (sd). Transkranielle Photobiomodulation verbessert die Kapazität des visuellen Arbeitsgedächtnisses beim Menschen. Wissenschaftliche Fortschritte, 8(48), eabq3211. https://doi.org/10.1126/sciadv.abq3211

